Warum Amylose im Gegensatz zu Amylopektin wasserlöslich ist?
Dagegen ist Amylose sehr gut wasserlöslich, weil aufgrund der weitausladenden Spiralstruktur die Ausbildung von kristallinen Bereichen erschwert ist und die Hydroxylgruppen mit dem Wasser Wasserstoffbrücken-Bindungen eingehen.
Warum Amylose im Gegensatz zu Amylopektin wasserlöslich?
Ich bin zu dem Ergebnis gekommen, dass Amylopektin besser löslich sein muss, da durch die reine Helix-Struktur der Amylose etliche polare Anteile des Moleküls "abgedeckt" sind. Im Amylopektinmolekül dagegen sind an den Verzweigungsstellen die polaren Anteile noch frei zugänglich.
Ist Amylose in Wasser löslich?
Amylose ist etwas in Wasser löslich; kolloidal löst sie sich gut in heißem Wasser. Amylosepasten bilden ein Gel aus und neigen zur Retrogradation. Durch Zugabe von Lugolscher Lösung färbt sich Amylose blau („Lugolscher Stärkenachweis“).
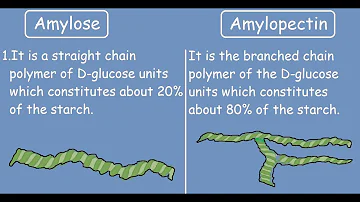
Was ist der Unterschied zwischen Amylose und Amylopektin?
Amylopektin, der Hauptbestandteil in den Stärkekörnern, besteht aus großen, stark verzweigten Molekülen. Amylose hingegen liegt in langen, kettenförmigen Molekülen vor.
Warum löst sich Stärke nicht in Wasser?
Stärke besteht aus winzigen Körnchen, die sich nicht in kaltem Wasser lösen.
Warum ist Amylose nicht wasserlöslich?
Dagegen ist Amylose sehr gut wasserlöslich, weil aufgrund der weitausladenden Spiralstruktur die Ausbildung von kristallinen Bereichen erschwert ist und die Hydroxylgruppen mit dem Wasser Wasserstoffbrücken-Bindungen eingehen.
Warum ist Stärke in heißem Wasser löslich?
In kaltem Wasser ist sie nur sehr schwer löslich, in heißem ist Stärke teilweise löslich (nämlich die Amylose) und quellfähig. Ab Temperaturen von etwa 68°C bildet sich aus dem Amylopektin ein Stärkekleister.
Welche Eigenschaften hat Amylose?
Amylose hat eine unverzweigte, schraubenartige Struktur (Wendel: etwa fünf bis sechs Glucosemoleküle pro Windung) und löst sich kolloid in heißem Wasser. Diese Windungen werden als Helix bezeichnet. Amylosepasten bilden ein Gel (Pudding) aus und neigen zur Retrogradation.
Was ist der Unterschied zwischen Amylose und Amylase?
α-Amylase (EC 3.2.1.1) spaltet die α(1-4)-Glykosidbindung der Amylose. Dadurch entstehen Dextrine und daraus Maltose, Glucose und verzweigte Oligosaccharide. β-Amylase (EC 3.2.1.2) spaltet vom Kettenende her jeweils ein Maltosemolekül nach dem anderen ab.
Warum quillt Stärke in Wasser auf?
Ihr Aggregatszustand ist fest. Sie ist in kaltem Wasser unlöslich. Beim Erhitzen kann sie an Wasser binden. Dadurch quillt sie auf und es entsteht Stärkekleister (Verkleisterung).
Warum ist Amylose in warmen Wasser löslich?
Dagegen ist Amylose sehr gut wasserlöslich, weil aufgrund der weitausladenden Spiralstruktur die Ausbildung von kristallinen Bereichen erschwert ist und die Hydroxylgruppen mit dem Wasser Wasserstoffbrücken-Bindungen eingehen.
Warum lösen sich Stoffe in heißem Wasser schneller als in kaltem Wasser?
Mit zunehmender Temperatur bewegen sich die kleinen Teilchen immer schneller. Dadurch treffen in heißem Wasser die Wasserteilchen häufiger und schneller auf die Farbstoff-Teilchen als in kaltem Wasser und lösen die Farbstoff-Teilchen sehr schnell aus ihrem Teilchenverbund heraus.
Welches Enzym spaltet Amylopektin?
Enzymatischer Abbau von Amylopektin
Die Spaltung (Hydrolyse) der α-1,6-glykosidischen Bindungen erfolgt durch das Enzym Amylo-1,6-Glucosidase.
Warum werden Amylasen erst bei Zugabe von Wasser wirksam?
Die Eiweißhäutchen um die Stärke reißen auf und ermöglichen ein Quellen der Stärke. Sie kann nun bis zu 30% ihres Eigengewichtes an Wasser aufnehmen. Dadurch wird sie für die Amylasen angreifbar.
Welches Enzym spaltet Amylose?
α-Amylase
α-Amylase (EC 3.2.1.1) spaltet die α(1-4)-Glykosidbindung der Amylose. Dadurch entstehen Dextrine und daraus Maltose, Glucose und verzweigte Oligosaccharide.
Warum ist Glucose so gut wasserlöslich?
In jedem Glucose-Molekül sind fünf Hydroxygruppen vorhanden, die mit dem Lösemittel Wasser Wasserstoffbrückenbindungen eingehen. Auch in dem Saccharose-Molekül sind trotz einer α-1,2-glykosidischen Bindung viele Hydroxygruppen vorhanden, die zur sehr guten Wasserlöslichkeit des Haushaltszuckers führen.
Warum löscht warmes Wasser besser als kaltes?
A: Löschen mit Wasser beruht auf zwei Wirkungen: Erstens entzieht das Wasser dem Brandherd Energie. Zweitens: Der entstehende Wasserdampf verhindert den Zutritt von Sauerstoff. Letzteres ist wichtiger für die Brandlöschung. Da warmes Wasser eher verdampft als kaltes, ist es wirksamer.
Welcher Stoff löst sich am besten im Wasser?
- Doch welche Stoffe lösen sich überhaupt in Wasser? Salze, Zucker und Alkohol sind Beispiele, bei denen Wasser gut als Lösungsmittel dient, während andere Stoffe wie Benzin oder Steine nicht im Wasser löslich sind.
Warum kann Amylase nur Stärke verdauen?
Die Amylase spaltet die Stärke (Polysaccharid) zu Dextrinen (Bruchstücke der Stärke). Je länger gekaut wird, desto kleiner wird das Stärkemolekül gespalten. Bei sehr langem Kauen bis zum Disaccharid Maltose. Im Magen wird die Alpha-Amylase aus dem Mundspeichel durch das saure Millieu zerstört.
Was hemmt Amylase?
- Amylasen arbeiten wie alle Enzyme nur in einem bestimmten pH-Wert-Bereich (Optimum alpha A.: 5,7 beta A.: 5,5), und werden im (stark) sauren Milieu deaktiviert, funktionieren also bei starker Ausschüttung von Magensäure (zur Eiweiß-Denaturierung) im Magen nicht. Ebenso können Fruchtsäuren die Enzyme hemmen.
Warum spaltet Amylase Stärke?
Amylase und seine Funktionen
Mit der Speichel-Amylase beginnt die Verdauung im Mund. Sie wird dann im Dünndarm durch die Pankreas-Amylase, ein Bestandteil des Pankreassaftes, fortgesetzt. Amylase macht Kohlenhydrate aus der Nahrung für den Körper verwertbar und baut sie zu kurzkettiger Stärke, Glykogen und Dextrin, ab.
Warum löst sich Glucose besser in Wasser als Stärke?
In jedem Glucose-Molekül sind fünf Hydroxygruppen vorhanden, die mit dem Lösemittel Wasser Wasserstoffbrückenbindungen eingehen. Auch in dem Saccharose-Molekül sind trotz einer α-1,2-glykosidischen Bindung viele Hydroxygruppen vorhanden, die zur sehr guten Wasserlöslichkeit des Haushaltszuckers führen.
Warum löst sich Zucker in Wasser und Öl nicht?
Die länglichen Ölteilchen können den Zucker nicht lösen, weil dieser nicht aus länglichen Teilchen besteht, sondern – das zeigt der Lösevorgang im Wasser – über ähnliche Strukturen verfügt wie das Wasser, nämlich über kugelige Anteile.
Warum darf man heißes Öl nicht mit Wasser löschen?
Fett und Wasser mischen sich nicht, das Wasser verdampft schlagartig und der entstehende Wasserdampf reißt kleine Fetttröpfchen mit. Diese entzünden sich, eine gewaltige Stichflamme ist das Ergebnis. Niemals darf man versuchen brennendes Fett mit Wasser zu löschen!
Warum soll man kein warmes Wasser aus der Leitung trinken?
Warmes Wasser aus der Warmwasserleitung zu trinken ist nur bedingt empfehlenswert. Denn es hat sich durch die Zirkulation im Warmwassersystem länger in den Rohren aufgehalten. Die Zirkulation ist notwendig, damit es überall heiß genug aus dem Wasserhahn kommt, um Legionellenbildung zu vermeiden.
Warum sind manche Stoffe wasserlöslich und andere nicht?
Da Wasser ein polares Lösungsmittel ist, sind in der Regel Stoffe gut in Wasser löslich, die ebenfalls polar sind. Dazu zählen Salze, Zucker und Alkohole. Unpolare Stoffe wie Sand, Benzin oder Öl sind unpolar und daher nicht in Wasser löslich.
